新薬承認申請に抗原性のデータが必須であるか否かの詮議はさておき,何故新薬の抗原性を検討しなければならないかを考えることにより,その必要性についての回答が得られると考える。即ち,一般合成医薬品はヒトにとっては異物であり,再投与されることにより薬物アレルギーを惹き起こす可能性を秘めている。一旦獲得された薬物アレルギーは生体に記憶され,生涯消されることはない。従って,全ての医薬品に対して抗原性を検討することが望まれる。因みに,海外において取下げられた上市品の原因の中で最も頻度の高い副作用は全身性過敏症で,その副作用の占める割合は全体の15%と高い頻度を示している1,2)。現在使用されている抗原性の検出試験としては,外用剤については予知性の高いモルモットのMaximization試験ならびにマウス局所リンパ節試験(Local Lymph Node Assay)があるが,全身投与を目的とした医薬品については一般にモルモットのActiveSystemic Anaphylaxis (ASA)およびPassive CutaneousAnaphylaxis (PCA)試験が使用されている。しかしながら,全身投与を目的とした後者の試験は高分子医薬品の抗原性の検出には適しているが,低分子医薬品の抗原性の検出には次の理由により適していない。即ち,その低分子医薬品が感作能を有していたとしても,一般に低分子医薬品の場合その分子上に抗原決定基は複数存在しないため,感作動物に当該低分子医薬品を再投与しても特異抗体との結合は起きるが,それ以後の補体の活性化を含む一連の反応は発現せず,高分子医薬品で見られる特異的なアナフィラキシー反応は誘発されない。従って,低分子医薬品の場合,高分子医薬品と同じ操作を行ってもその抗原性(感作能および反応惹起能)を検出することは甚だ難しい。
諸外国でも,低分子医薬品に対しては適切な試験法がないということから,抗原性の検討は原則として要求していない。本邦においても,このような現況から,上述のごとく安全性の検討項目から抗原性が削除され,「その他の毒性」に移され,必要に応じて実施する検討項目に位置付けられた。しかしながら,モルモットの試験も,低分子医薬品を投与した動物の感作リンパ球をin vitroにて同一薬物と共に培養し,3H-thymidineの取り込みを無処置リンパ球の取り込みと比較することにより,その医薬品が感作能を有しているか否かを予知することは出来る3) (Fig. 1参照)。
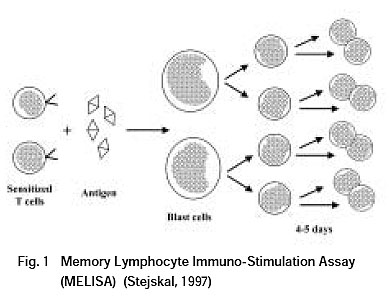
海外においては,全身的に投与された医薬品によるアレルギーあるいは自己免疫反応を検出する試験系としてマウス膝下リンパ節試験(PLNA)4-10)が報告されており,開発医薬品の抗原性試験に応用されている11-14)(Table 1)。

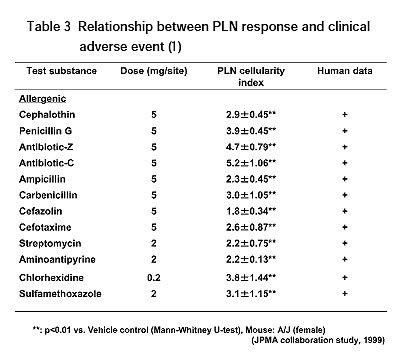
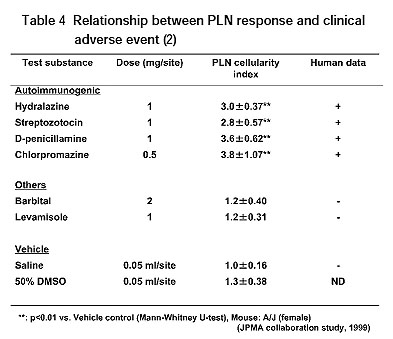
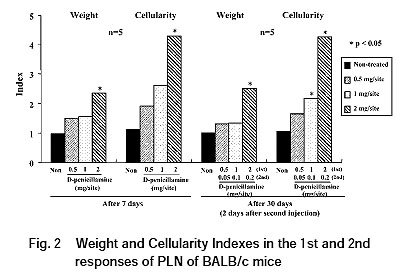
本邦においても,日本製薬工業協会の共同研究により,臨床で薬物アレルギーの誘発が知られている医薬品を用い,PLNA反応との相関性が検討された。その結果,明確にPLNA反応との相関性が証明されたことから,PLNAは低分子医薬品の抗原性の予知に応用できることが確認され13-17),低分子医薬品の抗原性の予知に利用可能と考えられた(Table 2-4)。しかし,PLNAと云えども万能な試験系ではなく,幾つかの留意点(皮膚刺激性を有する濃度では擬陽性を示すが,刺激反応と免疫反応の区別は2次応答反応の有無で確認可能であること(Fig. 2参照)および代謝物が抗原性の本体である場合,代謝物を使用する必要があること)があるが,十分にその留意点を理解した上で用いれば利用価値のある試験と考えられる。PLNAは,モルモット試験のように症状観察で評価する試験ではないため,どの程度強い薬物アレルギー反応が誘発されるのかは予測できないが,その医薬品の抗原性(感作能)あるいは自己免疫性の有無の予知は可能である。

抗原性試験に関しては準拠すべきガイドラインがないことから,それぞれの企業が自主的に適切な試験方法を選択し,開発医薬品の抗原性を検討することが出来る。この点については,医薬品研究(2003)の「毒性Q&A」に同様の記載があり,更に,既に諸外国で十分な臨床経験のある医薬品の場合,その薬物アレルギーに関する情報は有用な抗原性の評価資料になり,PLNAといった新しい試験方法の成績,すべての安全性試験データや臨床試験データ,類薬情報から総合的に判断し,ヒトにおいて重篤な薬物アレルギーを未然に防止することを勧めている18)。
従って,高分子医薬品については,従来通りモルモットを使用した抗原性試験を実施すればよいが,低分子医薬品については,被験医薬品投与モルモットのリンパ球幼若化試験やPLNAを実施し,陽性反応を示す成績が得られた場合は,被験医薬品の他剤との交叉性ならびに薬剤起因性自己免疫疾患の発現の可能性を考慮して臨床試験を実施することが必要であると考える。
[文献]
1) deWeck AL: Immunopathological mechanisms andclinical aspects of allergic reactions to drugs, indeWeck AL, Bundgaard H (eds) (1983): Handbook ofExperimental Pharmacology: Allergic Reactions toDrugs. New York: Springer-Verlag, pp 75-133
2) Guzzie PJ (1995): Immunotoxicology in pharmaceuticaldevelopment. In Gad SC (ed): Safety Assessment forPharmaceuticals. New York: Wiley, pp 325-385
3) Stejskal VDM (1997): Human hapten-specificlymphocytes: Biomarkers of allergy in man. DrugInformation Journal, 31: 1379-1382
4) Albers R et al. (1997): Suitability of the popliteal lymphnode assay as a predictive immunotoxicicological test.Drug Information Journal 31: 1337-1340
5) Hurtenbach U et al. (1987): Immunity to D-penicillamine: genetic, cellular, and chemicalrequirements for induction of popliteal lymph nodeenlargement in the mouse. J Immunol 139(2): 411-416
6) Kammuller ME et al. (1989): The popliteal lymph nodeassay in mice to screen for the immune disregulatingpotential of chemicals--a preliminary study. Int JImmunopharmacol 11(3): 293-300
7) Patriarca C et al. (1994): Comparison of popliteal lymphnode responses in various strains of rats. Hum ExpToxicol 13(7): 455-460
8) Bloksma N et al. (1995): Predictive immunotoxicologicaltest systems: Suitability of the popliteal lymph nodeassay in mice and rats. Crit Rev Toxicol 25(5): 369-396
9) Goebel C et al. (1996): The popliteal lymph node assay inmice: Screening of drugs and other chemicals forimmunotoxic hazard. Inflamm Res 45(Suppl 2): S85-S9
10) Pieters R et al. (2002): Predictive testing forautoimmunity. Toxicol Lett 127(1-3):83-91
11) Pieters R (2001):The popliteal lymph node assay: Atool for predicting drug allergies. Toxicology 158(1-2):65-69
12) Gutting BW et al. (2002): Investigating the TNP-OVAand direct popliteal lymph node assays for thedetection of immunostimulation by drugs associatedwith anaphylaxis in humans. J Appl Toxicol 22(3): 177-183
13) Gutting BW et al. (2002): Diclofenac activates T cellsin the direct popliteal lymph node assay and selectivelyinduces IgG1and IgE against co-injected TNP-OVA.Toxicol Lett 131(3): 167-180
14) Gutting BW et al. (2002):BALB/c mice orallypretreated with diclofenac have augmented andaccelerated PLNA responses to diclofenac. Toxicology172(3): 217-230
15) Aida T et al. (1998): Evaluation of allergenic potentialof low-molecular compounds by mouse popliteal lymphnode assay. J Toxicol Sci 23(5): 425-432
16) Shinkai K et al. (1999): Mouse popliteal lymph nodeassay for assessment of allergic and autoimmunity-inducing potentials of low-molecular-weight drugs. JToxicol Sci 24(2): 95-102
17) Suda A et al. (2000): Differentiation of responses toallergenic and irritant compounds in mouse popliteallymph node assay. J Toxicol Sci 25(2): 131-136
18) 医薬品医療機器審査センター(2003):毒性Q&A.医薬品研究, 34(11): 753-755